UDI Zertifikatstypen
Jedes in Europa verkaufte Medizinprodukt benötigt ein gültiges Zulassungszertifikat gemäß MDR 2017/745 und IVDR 2017/746. Es bescheinigt, dass das Produkt alle gesetzlichen Anforderungen an ein Medizinprodukt erfüllt. Durch die Zusammenfassung einer Produktgruppe zu einer Basis UDI-DI wird nur ein Zertifikat für eine Produktgruppe benötigt, anstatt für jeden Artikel innerhalb einer Produktgruppe. Der Zertifikatstyp gibt den Typ des mit dem Gerät verbundenen Produktzertifikats an.
Für die FDA sind UDI Zertifikatstypen momentan nicht relevant.
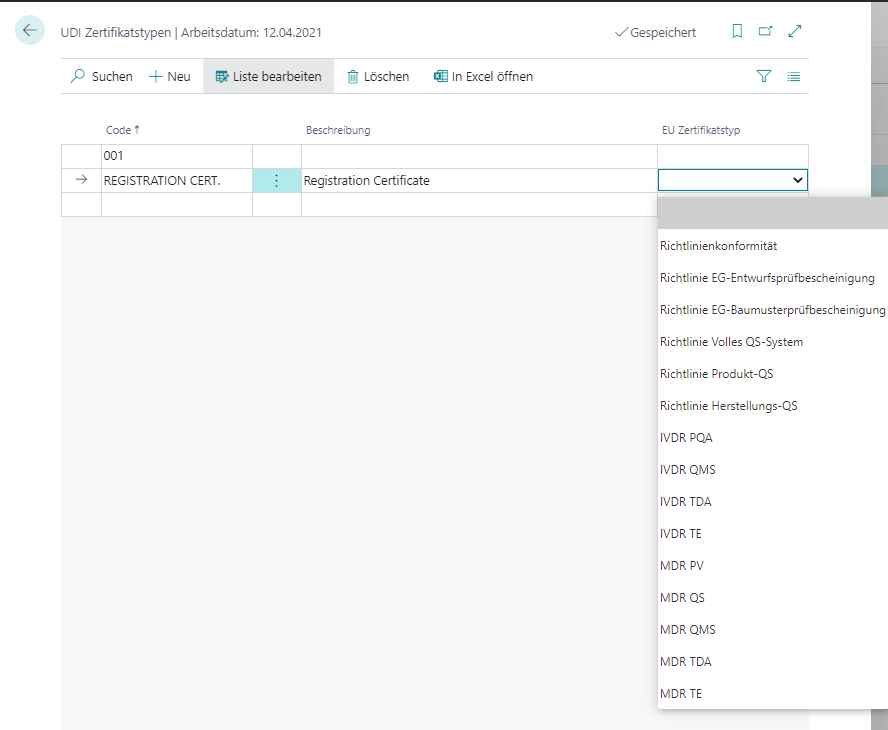
| Feld | Beschreibung |
|---|---|
| Code | Gibt einen Zertifikatstyp Code an, den Sie auswählen können. |
| Beschreibung | Gibt einen Text zur Beschreibung des Zertifikatstyps an. |
| EU Zertifikatstyp | Gibt den Zertifikatstyp an, welcher beim Export zur EUDAMED verwendet wird. |
Feedback
Senden Sie Feedback für diese Seite. (Beachten Sie, dass diese Umfrage auf Englisch ist.)